⏱️ สรุปสาระสำคัญใน 1 นาที
- มะเร็งระยะลุกลาม: ไม่ใช่จุดจบ แต่คือการเปลี่ยนเป้าหมายจาก “การรักษาให้หายขาด” เป็น “การควบคุมโรคและรักษาคุณภาพชีวิต” เพื่อให้ผู้ป่วยใช้ชีวิตอยู่ได้อย่างปกติที่สุด
- กลไกการแพร่กระจาย: มะเร็งไม่ได้ลามแบบสุ่ม แต่มีลำดับขั้นตอนเหมือน “การแหกคุก” โดยใช้เกล็ดเลือดพรางตัวจากภูมิคุ้มกัน และใช้โปรตีนหลอก (PD-L1) เพื่อไม่ให้ถูกทำลาย
- การตรวจแบบแม่นยำ (Liquid Biopsy): ตรวจหาเซลล์มะเร็งในเลือด (CTCs) เพื่อดู “หน้าตาปัจจุบัน” ของมะเร็ง ซึ่งเปลี่ยนไปจากการตรวจชิ้นเนื้อครั้งแรก ทำให้เลือกยาได้ตรงจุดกว่า
- นวัตกรรมที่ RoyalLee: เน้นการภูมิคุ้มกันบำบัด (เช่น NK Cell, ICB) เพื่อ “ถอดหน้ากาก” มะเร็ง และส่งสัญญาณให้ร่างกายกลับมาทำลายเซลล์ร้ายได้ด้วยตัวเอง
- 1. กลไกการแพร่กระจาย (The Metastatic Cascade)
- 2. บทบาทของ TGF-β: สัญญาณที่เปลี่ยนข้างในมะเร็งระยะลุกลาม
- 3. ปัจจัยที่ทำให้มะเร็งระยะแพร่กระจายมีความซับซ้อน และรับมือยาก?
- 4. การปรับเป้าหมาย: ควบคุมโรคและมุ่งเน้น ‘คุณภาพชีวิต’
- อธิบายแต่ละแผง
- 5. RoyalLee ประเมินและวางแผนการรักษามะเร็งระยะลุกลามให้คุณได้อย่างไร
- กระบวนการประเมินก่อนเริ่มการรักษาที่ RoyalLee
- คำถามที่พบบ่อย (FAQ)
- แหล่งข้อมูลอ้างอิง
การก้าวเข้าสู่ภาวะมะเร็งระยะลุกลาม หรือระยะแพร่กระจาย (Metastasis) คือการเปลี่ยนแปลงที่สำคัญของพยาธิสภาพโรค ในระยะนี้ความซับซ้อนทางการแพทย์จะเพิ่มสูงขึ้น การทำความเข้าใจกลไกทางชีววิทยาและข้อจำกัดของการรักษาอย่างตรงไปตรงมา คือข้อมูลพื้นฐานที่จำเป็นสำหรับการวางแผนรับมือ
ที่ RoyalLee Cancer Hospital Guangzhou เรานำเสนอข้อเท็จจริงทางการแพทย์โดยไม่ใช้ความหวังที่เลื่อนลอย ภายใต้ปรัชญา เราเคารพในชีวิต (Respecting Life) การตัดสินใจที่ถูกต้องต้องมาจากข้อมูลที่แม่นยำ เพื่อให้เป้าหมายของการรักษาสอดคล้องกับ ‘คุณภาพชีวิต’ ซึ่งเป็น ‘หัวใจ’ ของทุกการตัดสินใจทางการแพทย์
1. กลไกการแพร่กระจาย (The Metastatic Cascade)
การลุกลามของมะเร็งไม่ใช่สิ่งที่เกิดขึ้นแบบสุ่ม แต่เป็นกระบวนการทางชีววิทยาที่เป็นลำดับขั้น (Metastatic Cascade) ซึ่งงานวิจัยในระยะหลังให้ความสนใจเป็นพิเศษกับ เซลล์มะเร็งที่หลุดเข้าสู่กระแสเลือด (Circulating Tumor Cells — CTCs) ในฐานะตัวกลางสำคัญของกระบวนการนี้
การเดินทางของเซลล์มะเร็ง: จากจุดเริ่มต้นสู่การยึดครองพื้นที่ใหม่
- การแหกคุก (Local Invasion): เซลล์มะเร็งผลิตเอนไซม์เพื่อย่อยสลายเนื้อเยื่อรอบๆ เหมือนการใช้สว่านพังกำแพงคุกออกมา
- การใช้ทางด่วน (Intravasation): เซลล์มะเร็งแทรกตัวเข้าสู่หลอดเลือดหรือหลอดน้ำเหลือง เราเรียกเซลล์เหล่านี้ว่า CTCs (Circulating Tumor Cells) ซึ่งเปรียบเสมือน “นักโทษที่หลบหนีอยู่บนทางด่วน”
- การพรางตัวจากตำรวจ (Circulation): ในกระแสเลือดจะมีภูมิคุ้มกัน (ตำรวจ) คอยตรวจจับ เซลล์มะเร็งจึงมักจะไปเกาะกับ “เกล็ดเลือด” เพื่อใช้เป็นหน้ากากพรางตัว ทำให้ภูมิคุ้มกันมองไม่เห็นว่าเป็นสิ่งแปลกปลอม
- การตั้งรกรากใหม่ (Secondary Tumor Formation): เมื่อไปถึงอวัยวะปลายทาง (เช่น ปอด ตับ หรือกระดูก) มันจะเริ่มสร้างหลอดเลือดใหม่เพื่อดึงสารอาหารมาเลี้ยงตัวเอง และเติบโตเป็นก้อนมะเร็งก้อนใหม่
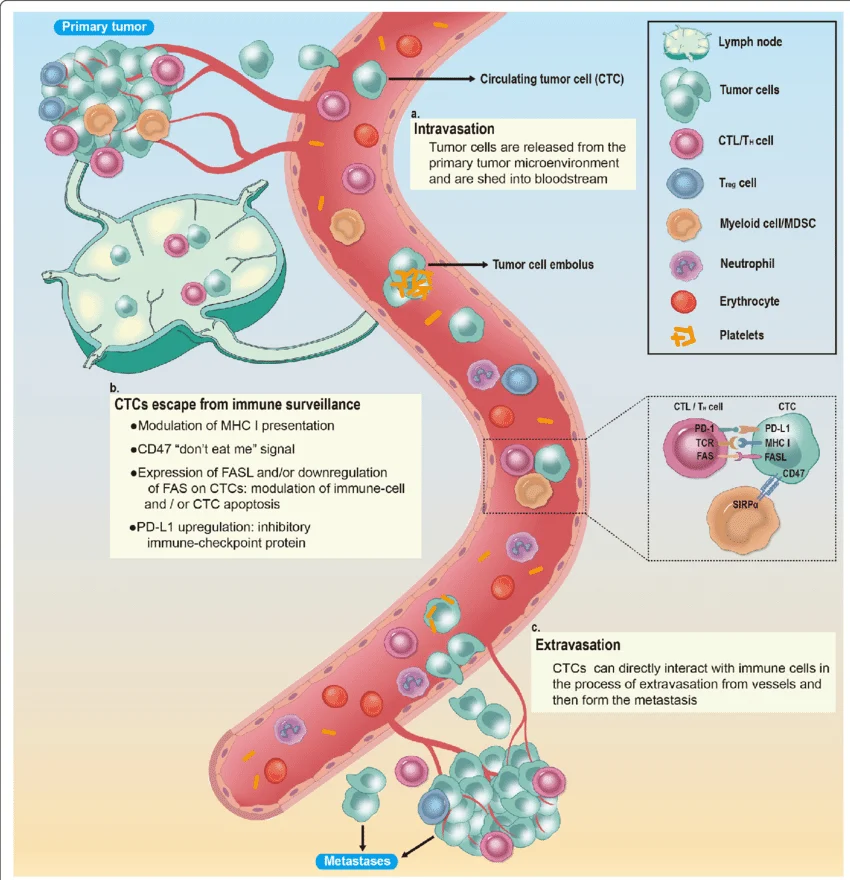
- (a) การเข้าสู่กระแสเลือด (Intravasation) — เซลล์มะเร็งหลุดจากก้อนมะเร็งต้นกำเนิดและกลายเป็น CTCs ในกระแสเลือด
- (b) การหลบหลีกภูมิคุ้มกัน (Immune Evasion) — CTCs ใช้กลไกต่างๆ เช่น CD47, PD-L1 และการลด MHC-I เพื่อหลีกเลี่ยงการถูกทำลาย และ
- (c) การออกจากหลอดเลือดและก่อตัวเป็นก้อนมะเร็งใหม่ (Extravasation and Metastasis)
ขั้นตอนหลักของ Metastatic Cascade (แบบเต็ม)
- การลุกลามเฉพาะที่ (Local Invasion) เซลล์มะเร็งแทรกตัวผ่านเนื้อเยื่อปกติรอบก้อนมะเร็งต้นกำเนิด (Primary Tumor) โดยอาศัยเอนไซม์ที่ย่อยสลายเนื้อเยื่อเกี่ยวพัน เช่น Matrix Metalloproteinases (MMPs) ซึ่งถูกกระตุ้นได้จากทั้งเซลล์มะเร็งเองและเซลล์สนับสนุนในสภาพแวดล้อมของเนื้องอก
- การเข้าสู่ระบบไหลเวียน (Intravasation) เซลล์มะเร็งแทรกซึมเข้าสู่ผนังหลอดเลือดหรือหลอดน้ำเหลืองบริเวณใกล้เคียง กลายเป็น CTCs ที่ไหลเวียนในกระแสเลือด ช่วงนี้เซลล์มะเร็งต้องเผชิญกับภูมิคุ้มกันของร่างกายโดยตรง แม้เซลล์มะเร็งหลายพันเซลล์อาจหลุดเข้ากระแสเลือดในแต่ละวัน แต่ส่วนใหญ่ถูกทำลายโดยระบบภูมิคุ้มกัน — เฉพาะที่รอดและปรับตัวได้เท่านั้นที่จะก่อให้เกิดการแพร่กระจาย
- การเดินทางในกระแสเลือด (Circulation) CTCs เดินทางตามกระแสเลือดไปยังส่วนต่างๆ ของร่างกาย บางส่วนรวมตัวกับเกล็ดเลือด (Platelets) ซึ่งช่วยพรางตัวจากการถูกโจมตีโดยเซลล์ NK (Natural Killer cells) งานวิจัยของ Zhong และคณะ (2020) อธิบายว่าเกล็ดเลือดสามารถถ่ายโอน MHC class I ไปยังผิวของ CTCs ทำให้ระบบภูมิคุ้มกันจำแนกไม่ออกว่าเป็นเซลล์แปลกปลอม
- การหยุดและแทรกตัวออก (Arrest and Extravasation) CTCs หยุดที่หลอดเลือดฝอยของอวัยวะปลายทาง แล้วแทรกตัวผ่านผนังหลอดเลือดเข้าสู่เนื้อเยื่อใหม่ กระบวนการนี้ได้รับการอำนวยความสะดวกจากโปรตีน E-selectin และการยึดเกาะกับเซลล์บุผนังหลอดเลือด
- การสร้างก้อนมะเร็งใหม่ (Secondary Tumor Formation) เมื่อเซลล์มะเร็งฝังตัวในอวัยวะใหม่สำเร็จ มันจะเริ่มกระตุ้นการสร้างหลอดเลือดใหม่ (Angiogenesis) เพื่อนำสารอาหารมาหล่อเลี้ยง และเติบโตเป็นก้อนมะเร็งทุติยภูมิ (Secondary Tumor) กระบวนการนี้ถูกขับเคลื่อนบางส่วนโดยโปรตีน TGF-β ซึ่งกระตุ้นการสร้าง VEGF และ CTGF ที่จำเป็นต่อการก่อตัวของหลอดเลือดใหม่
2. บทบาทของ TGF-β: สัญญาณที่เปลี่ยนข้างในมะเร็งระยะลุกลาม
หนึ่งในปัจจัยทางชีววิทยาที่สำคัญที่สุดในการทำความเข้าใจมะเร็งระยะลุกลาม คือโปรตีนที่เรียกว่า Transforming Growth Factor-beta (TGF-β)
ปรากฏการณ์ “สายลับสองหน้า” (The TGF-β Paradox)
- ในระยะเริ่มต้น: มันทำหน้าที่เป็น “ตำรวจ” ช่วยกดไม่ให้เซลล์มะเร็งเติบโต
- ในระยะลุกลาม: เซลล์มะเร็งจะเรียนรู้วิธี “ซื้อตัว” ตำรวจคนนี้ให้กลายเป็น “สายลับ” ที่ช่วยมะเร็งแทน โดยมันจะสั่งให้ภูมิคุ้มกันในบริเวณนั้นหยุดทำงาน และช่วยเปลี่ยนรูปร่างเซลล์มะเร็งให้เคลื่อนที่ไปส่วนต่างๆ ได้ง่ายขึ้น
TGF-β มีบทบาทที่ดูย้อนแย้งในมะเร็ง งานวิจัยของ Cantelli และคณะ (2016) อธิบายปรากฏการณ์นี้ไว้ว่า ในระยะต้นของมะเร็ง TGF-β ทำหน้าที่เป็น “ผู้ยับยั้งเนื้องอก” (Tumor Suppressor) โดยกดการเติบโตและกระตุ้นการทำลายตนเองของเซลล์ผิดปกติ แต่เมื่อเซลล์มะเร็งพัฒนาและสะสมการกลายพันธุ์มากพอ มันจะสามารถ “ฉวยโอกาส” จาก TGF-β โดยใช้สัญญาณเดิมเพื่อส่งเสริมการลุกลามและหลบหลีกภูมิคุ้มกันแทน นักวิจัยเรียกปรากฏการณ์นี้ว่า “The TGF-β Paradox”
ในทางปฏิบัติ TGF-β ช่วยให้มะเร็งระยะลุกลามมีพลังมากขึ้นโดย:
- กระตุ้น EMT (Epithelial-Mesenchymal Transition): ทำให้เซลล์มะเร็งเปลี่ยนรูปร่างและได้รับความสามารถในการเคลื่อนที่ ซึ่งเป็นก้าวแรกที่จำเป็นของการแพร่กระจาย
- ยับยั้งระบบภูมิคุ้มกัน: TGF-β ลดประสิทธิภาพของเซลล์ภูมิคุ้มกันหลายชนิด ทั้ง NK cells, Cytotoxic T cells และ Dendritic cells ในเวลาเดียวกัน
- ส่งเสริมสภาพแวดล้อมที่เอื้อต่อมะเร็ง: กระตุ้นให้ fibroblasts และ macrophages ที่อยู่รอบเนื้องอกทำงานสนับสนุนการลุกลามของมะเร็งแทนที่จะต้านทานมัน
3. ปัจจัยที่ทำให้มะเร็งระยะแพร่กระจายมีความซับซ้อน และรับมือยาก?
- ความแตกต่างในตัวละคร (Tumor Heterogeneity): เซลล์มะเร็งที่แพร่กระจายไปที่ตับ อาจจะมีนิสัย (พันธุกรรม) ไม่เหมือนกับก้อนเดิมที่เต้านม ตัวอย่างเช่น: ยาที่เคยใช้ฆ่ามะเร็งที่เต้านมได้ผล อาจจะใช้ไม่ได้ผลเลยกับก้อนที่ไปโผล่ที่ตับ เพราะมันกลายพันธุ์ไปแล้ว
- การสร้างป้อมปราการ (Tumor Microenvironment): มะเร็งไม่ได้อยู่เฉยๆ แต่มันสร้างสภาพแวดล้อมรอบตัวให้เป็น “เขตอันตราย” ที่ยาเข้าถึงยาก หรือส่งสัญญาณหลอกว่า “อย่ากินฉัน” หรือ “อย่ามองหาฉัน” เพื่อให้ภูมิคุ้มกันปล่อยผ่านไป
ความหลากหลายทางพันธุกรรม (Tumor Heterogeneity)
เซลล์มะเร็งที่แพร่กระจายไปยังอวัยวะอื่นมักมีการกลายพันธุ์ที่แตกต่างไปจากก้อนต้นกำเนิด ส่งผลให้ยาที่เคยกดก้อนมะเร็งเดิมได้อาจไม่มีผลกับก้อนใหม่ นี่คือเหตุผลหนึ่งที่การตรวจชิ้นเนื้อ (Tissue Biopsy) จากจุดเดียวให้ภาพที่ไม่ครบถ้วนของโรค
CTCs จากเลือด (Liquid Biopsy) จึงเป็นทางเลือกที่น่าสนใจในการติดตามการเปลี่ยนแปลงของโรคแบบ real-time เพราะสะท้อนความหลากหลายของเซลล์มะเร็งในร่างกายได้ดีกว่า
สภาพแวดล้อมระดับจุลภาค (Tumor Microenvironment — TME)
เซลล์มะเร็งไม่ได้อยู่โดดเดี่ยว แต่สร้างสภาพแวดล้อมที่เอื้อต่อตัวเองโดยหลั่งสารต่างๆ กระตุ้นให้เซลล์ข้างเคียง เช่น fibroblasts, macrophages และเส้นเลือดใหม่ เข้ามาสนับสนุนการเติบโตและช่วยต้านทานการรักษา
การหลบหลีกภูมิคุ้มกัน (Immune Evasion)
CTCs ใช้กลไกหลายอย่างเพื่อหลบเลี่ยงการถูกทำลาย ที่สำคัญ ได้แก่:
- PD-L1: โปรตีนที่ส่งสัญญาณ “อย่ามองหาฉัน” (do not find me) ไปยัง T cells ทำให้ภูมิคุ้มกันหยุดโจมตี การตรวจพบ PD-L1 บน CTCs มีนัยสำคัญต่อการพยากรณ์โรคและการเลือกใช้ยา Immune Checkpoint Inhibitors
- CD47: โปรตีนที่ส่งสัญญาณ “อย่ากินฉัน” (do not eat me) ไปยัง macrophages ยับยั้งการถูกกำจัดโดย phagocytosis
- การลด MHC-I: ทำให้ Cytotoxic T cells จำแนกเซลล์มะเร็งไม่ได้และข้ามผ่านไป
4. การปรับเป้าหมาย: ควบคุมโรคและมุ่งเน้น ‘คุณภาพชีวิต’
เมื่อโรคเข้าสู่ระยะลุกลาม แนวทางจากสมาคมเนื้องอกวิทยาทางคลินิกแห่งสหรัฐอเมริกา (ASCO) แนะนำว่าเป้าหมายหลักของการรักษามักจะเปลี่ยนจากการ “รักษาให้หายขาด” (Curative) ไปสู่การ “ควบคุมโรค บรรเทาอาการ และรักษาคุณภาพชีวิต” (Palliative and Disease Management)
ที่ RoyalLee เราใช้แนวทาง Life-Aligned Oncology เพื่อประเมินทางเลือกที่เหมาะสมในแต่ละราย:
ประเมินผลกระทบ (Risk-Benefit Assessment) พิจารณาว่าผลข้างเคียงของการรักษาจะกระทบความสามารถในการใช้ชีวิตประจำวันของผู้ป่วยมากน้อยเพียงใด
การรักษาแบบจำเพาะเจาะจง ใช้การตรวจวิเคราะห์ระดับยีนและโมเลกุล รวมถึงการตรวจ CTCs จากเลือด เพื่อประเมินความคุ้มค่าของการใช้ยาพุ่งเป้า (Targeted Therapy) หรือภูมิคุ้มกันบำบัด (Immunotherapy) เช่น การตรวจสอบ PD-L1 บน CTCs ก่อนการใช้ Immune Checkpoint Inhibitors
การจัดการอาการ (Symptom Management) ให้ความสำคัญกับการลดความเจ็บปวดและรักษาการทำงานของอวัยวะสำคัญที่ถูกมะเร็งลุกลาม เพื่อให้ผู้ป่วยดำรงชีวิตด้วยคุณภาพที่ดีที่สุดเท่าที่จะเป็นไปได้
อธิบายแต่ละแผง
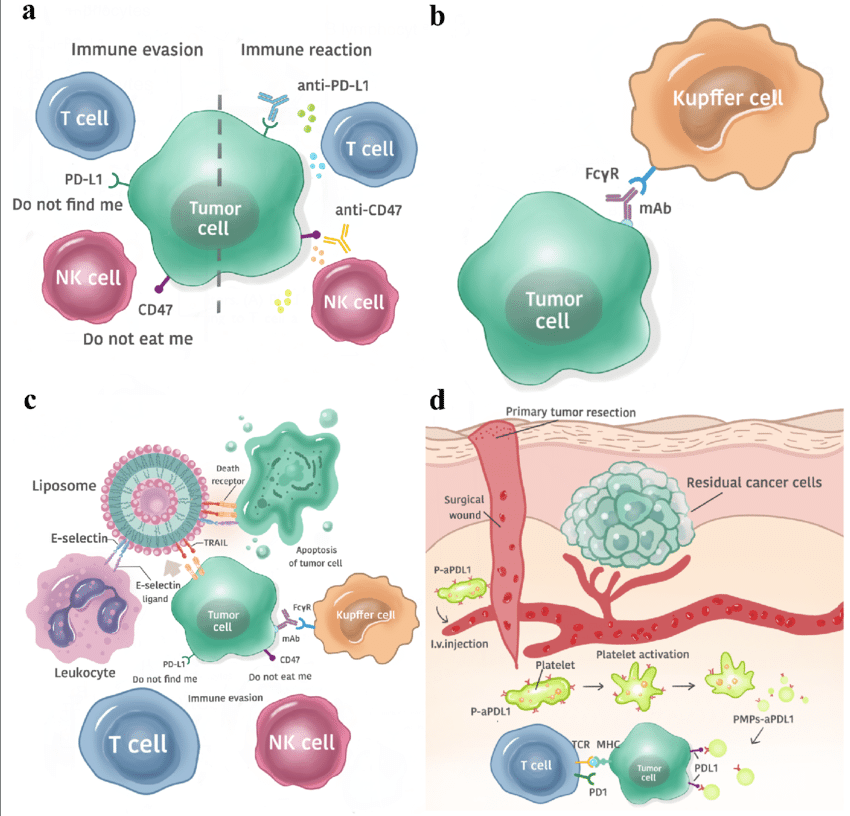
สี่กลยุทธ์ภูมิคุ้มกันบำบัดที่มุ่งเป้าที่เซลล์มะเร็งในกระแสเลือด (CTCs) ได้แก่ (a) การบล็อก immune checkpoint คู่ PD-L1/CD47 (b) การใช้ monoclonal antibody กระตุ้น Kupffer cell ในตับ (c) การใช้เม็ดเลือดขาวเป็นพาหนะส่ง TRAIL เข้าโจมตี CTC และ (d) การใช้เกล็ดเลือดส่ง anti-PD-L1 ไปยังบาดแผลหลังผ่าตัดเพื่อป้องกันการกลับมาของโรค
(a) Immune Checkpoint Therapy — ปลดล็อกภูมิคุ้มกัน
เซลล์มะเร็งใช้โปรตีน 2 ตัวเพื่อพรางตัว:
- PD-L1 → ส่งสัญญาณ “Do not find me” ไปยัง T cell
- CD47 → ส่งสัญญาณ “Do not eat me” ไปยัง NK cell
การใช้ยาบล็อกทั้งสองพร้อมกัน (anti-PD-L1 + anti-CD47) ปลดสัญญาณพรางตัว ทำให้ T cell และ NK cell กลับมาโจมตีเซลล์มะเร็งได้ งานวิจัยพบว่าการบล็อกคู่มีประสิทธิภาพดีกว่าบล็อกตัวใดตัวหนึ่งเพียงอย่างเดียว
(b) Monoclonal Antibody (mAb) Therapy — ใช้ Kupffer cell กำจัด CTC
ฉีด monoclonal antibody (mAb) เข้าร่างกาย แอนติบอดีจะจับผิวเซลล์มะเร็ง จากนั้น Kupffer cell (macrophage ประจำตับ) จะจดจำผ่าน receptor FcγR และกลืนกินเซลล์มะเร็งนั้น กลไกนี้สำคัญมากในการป้องกันการแพร่กระจายไปที่ตับ
(c) “Unnatural Killer Cell” Therapy — ใช้เม็ดเลือดขาวเป็นพาหนะ
แนวคิดแปลกใหม่คือการ เคลือบเม็ดเลือดขาว (Leukocyte) ด้วย liposome ที่บรรจุ:
- E-selectin — โปรตีนที่ช่วยให้เกาะติด CTC
- TRAIL — โปรตีนที่กระตุ้นให้เซลล์มะเร็งทำลายตัวเอง (apoptosis)
เหตุผลที่ใช้เม็ดเลือดขาวแทน liposome ลอยอิสระ คือใน bloodstream CTCs และ leukocytes อยู่ชั้นนอกของการไหล จึงสัมผัสกันบ่อยกว่ามาก ทำให้ TRAIL เข้าถึง CTC ได้มีประสิทธิภาพกว่า
(d) In vivo P-aPDL1 Therapy — ใช้เกล็ดเลือดส่งยา
หลังผ่าตัดเอาก้อนมะเร็งออก มักมี residual cancer cells หลงเหลืออยู่ในบาดแผล และ CTC ที่หมุนเวียนอยู่
กลยุทธ์นี้คือการจับ anti-PD-L1 (aPDL1) ติดกับผิวเกล็ดเลือด (Platelet) ฉีดเข้าเส้นเลือด เมื่อเกล็ดเลือดถูกกระตุ้นบริเวณแผล มันจะแตกตัวเป็น Platelet Microparticles (PMPs) ที่พา aPDL1 ไปบล็อก PD-L1 บน CTC และ residual cancer cells โดยตรง กระตุ้น T cell ให้โจมตีเซลล์ที่เหลืออยู่
5. RoyalLee ประเมินและวางแผนการรักษามะเร็งระยะลุกลามให้คุณได้อย่างไร
นวัตกรรมที่ RoyalLee การรบที่เจาะจงระดับโมเลกุล
ความเข้าใจกลไกของมะเร็งระยะลุกลามในระดับโมเลกุล คือจุดเริ่มต้นของการวางแผนการรักษาที่ตรงจุด ที่ RoyalLee Cancer Hospital Guangzhou เรามีทั้งเทคโนโลยีการวินิจฉัยและทางเลือกการรักษาครบวงจร ภายใต้ทีมแพทย์เฉพาะทางด้านมะเร็งวิทยาที่มีประสบการณ์จริง
ภูมิคุ้มกันบำบัด (Immunotherapy) — มุ่งเป้าที่กลไกหลบหลีกของ CTC โดยตรง
เมื่อเข้าใจแล้วว่า CTCs ใช้ PD-L1, CD47 และ MHC-I เป็นเครื่องมือหลบเลี่ยงภูมิคุ้มกัน การรักษาที่ได้ผลจึงต้องปลดล็อกกลไกเหล่านี้ RoyalLee มีบริการภูมิคุ้มกันบำบัดหลายรูปแบบที่ครอบคลุมแนวทางสมัยใหม่:
- Immune Checkpoint Blockade (IMMUNO_ICB) การใช้ยาต้าน PD-1/PD-L1 เพื่อปลดสัญญาณ “อย่ามองหาฉัน” บนผิว CTC ให้ T cells กลับมาจดจำและโจมตีเซลล์มะเร็งได้ตามปกติ เหมาะสำหรับผู้ป่วยที่ตรวจพบ PD-L1(+) CTCs ในกระแสเลือด
- NK Cell Therapy (IMMUNO_NK) การบำบัดด้วยเซลล์ Natural Killer (NK) ที่ถูกเตรียมและขยายจำนวนนอกร่างกาย แล้วนำกลับเข้าสู่ร่างกายเพื่อเพิ่มประสิทธิภาพในการตรวจจับและทำลาย CTC งานวิจัยพบว่า NK Cell Therapy ช่วยลดจำนวน CTC ในกระแสเลือดของผู้ป่วยมะเร็งปอดระยะที่ 4 ได้อย่างมีนัยสำคัญภายใน 30 วัน
- DC-T Cell Therapy (IMMUNO_DCT) การกระตุ้น Dendritic Cells (DCs) ให้นำเสนอแอนติเจนของเซลล์มะเร็งต่อ T cells เพื่อสร้างภูมิคุ้มกันจำเพาะต่อเนื้องอก เหมาะสำหรับผู้ป่วยที่ต้องการกระตุ้นการตอบสนองทางภูมิคุ้มกันแบบยั่งยืน
- Gamma-Delta T Cell Therapy (IMMUNO_GD) การใช้ Gamma-Delta T cells ซึ่งเป็นเซลล์ภูมิคุ้มกันที่สามารถโจมตีเซลล์มะเร็งได้โดยไม่ต้องอาศัย MHC-I presentation — ข้ามผ่านกลไกหลบเลี่ยงที่มะเร็งใช้กับ CTL ทั่วไปได้โดยตรง
- Novel Complex Immunotherapy (IMMUNO_COMPLEX) การผสมผสานหลายกลยุทธ์ภูมิคุ้มกันบำบัดเข้าด้วยกัน ออกแบบเป็น protocol เฉพาะบุคคลตามผลการตรวจโมเลกุลและสภาวะภูมิคุ้มกันของผู้ป่วย
- TIL Therapy (IMMUNO_TIL) การนำเซลล์ภูมิคุ้มกันที่แทรกซึมเข้าไปในก้อนมะเร็ง (Tumor-Infiltrating Lymphocytes) ออกมาขยายจำนวนนอกร่างกาย แล้วนำกลับเข้าสู่ผู้ป่วยในปริมาณที่มากกว่าเดิมหลายร้อยเท่า เป็นหนึ่งในแนวทางที่ได้รับความสนใจสูงในมะเร็งระยะลุกลามหลายชนิด
- Cancer Stem Cell Vaccine (IMMUNO_VACCINE) วัคซีนที่มุ่งเป้าที่ Cancer Stem Cells ซึ่งเป็นเซลล์รากของมะเร็งที่มีความทนทานสูงและเป็นสาเหตุหลักของการกลับมาของโรคหลังการรักษา
กระบวนการประเมินก่อนเริ่มการรักษาที่ RoyalLee
RoyalLee ไม่แนะนำการรักษาโดยไม่มีข้อมูลเพียงพอ กระบวนการเริ่มต้นด้วยการประเมินที่ครอบคลุม:
- ขั้นที่ 1 — ตรวจวิเคราะห์ระดับโมเลกุล ตรวจ CTC จากเลือด (Liquid Biopsy) เพื่อประเมิน PD-L1 expression, CD47 expression และโปรไฟล์ทางพันธุกรรมของเซลล์มะเร็งที่หมุนเวียนอยู่ในร่างกาย — ข้อมูลที่การตรวจชิ้นเนื้อเพียงจุดเดียวให้ไม่ได้
- ขั้นที่ 2 — ประเมินสภาวะภูมิคุ้มกัน วิเคราะห์สัดส่วนและประสิทธิภาพของเซลล์ภูมิคุ้มกันในร่างกาย เพื่อดูว่าผู้ป่วยเหมาะกับภูมิคุ้มกันบำบัดรูปแบบใดมากที่สุด
- ขั้นที่ 3 — ออกแบบแผนการรักษาเฉพาะบุคคล ทีมแพทย์หลายสาขา (Multidisciplinary Team) ร่วมกันออกแบบแผนที่ผสมผสานทางเลือกที่เหมาะสม โดยคำนึงถึงทั้งประสิทธิผลและคุณภาพชีวิตของผู้ป่วย
- ขั้นที่ 4 — ติดตามผลและปรับแผน วัดผลการรักษาด้วยการตรวจ CTC ซ้ำเพื่อดูการเปลี่ยนแปลงของโรค และปรับ protocol ตามการตอบสนองจริง
การรู้ว่าร่างกายของคุณตอบสนองต่อการรักษาแบบใด คือความได้เปรียบที่แท้จริงในการรับมือกับมะเร็งระยะลุกลาม
ปรึกษาทีมแพทย์ RoyalLee Cancer Hospital Guangzhou เพื่อรับการประเมินที่ตรงกับสภาวะของคุณ — ไม่ใช่แผนสำเร็จรูป แต่เป็นแผนที่ออกแบบมาเพื่อคุณโดยเฉพาะ
คำถามที่พบบ่อย (FAQ)
Q: เซลล์มะเร็งเต้านมที่ลุกลามไปที่กระดูก ถือว่าเป็นมะเร็งกระดูกหรือไม่?
ไม่ใช่ครับ/ค่ะ มะเร็งที่แพร่กระจายจะยังคงถูกเรียกชื่อตามอวัยวะต้นกำเนิดเสมอ กรณีนี้เรียกว่า “มะเร็งเต้านมระยะแพร่กระจายไปที่กระดูก” (Metastatic Breast Cancer to Bone) ลักษณะของเซลล์และแนวทางการรักษาหลักยังคงมุ่งเป้าที่เซลล์มะเร็งเต้านม ไม่ใช่เซลล์กระดูก
Q: มะเร็งระยะลุกลาม (Metastatic Cancer) รักษาให้หายขาดได้หรือไม่?
ในมุมมองทางการแพทย์ปัจจุบัน มะเร็งระยะแพร่กระจายส่วนใหญ่ไม่สามารถรักษาให้หายขาดได้ มีข้อยกเว้นบางส่วน เช่น มะเร็งผิวหนัง (Melanoma) และมะเร็งปอดชนิด Non-Small Cell บางราย ที่ตอบสนองต่อ Immunotherapy ได้อย่างยั่งยืน การรักษาโดยทั่วไปจึงมุ่งเน้นที่การชะลอการเติบโตของโรค ยืดอายุขัย และรักษาคุณภาพชีวิต
Q: Liquid Biopsy หรือการตรวจ CTCs จากเลือด คืออะไร และมีประโยชน์อย่างไร?
Liquid Biopsy คือการตรวจเลือดเพื่อหา CTCs หรือ DNA จากเซลล์มะเร็ง (Circulating Tumor DNA) ข้อดีคือไม่รุกล้ำร่างกาย ทำซ้ำได้บ่อยเพื่อติดตามการเปลี่ยนแปลงของโรค และสะท้อนความหลากหลายของเซลล์มะเร็งในร่างกายได้ดีกว่าการตรวจชิ้นเนื้อจากจุดเดียว ปัจจุบันมีการใช้ในการประเมินการตอบสนองต่อ NK cell therapy และ Immune Checkpoint Inhibitors
แหล่งข้อมูลอ้างอิง
- National Cancer Institute (NCI). Metastatic Cancer: When Cancer Spreads. https://www.cancer.gov/
- American Society of Clinical Oncology (ASCO). Advanced Cancer Care and Palliative Care Guidelines. https://www.asco.org/
- Zhong X, Zhang H, Zhu Y, et al. (2020). Circulating tumor cells in cancer patients: developments and clinical applications for immunotherapy. Molecular Cancer, 19(1), 15. https://doi.org/10.1186/s12943-020-1141-9
- Cantelli G, Crosas-Molist E, Georgouli M, Sanz-Moreno V. (2016). TGFB-induced transcription in cancer. Seminars in Cancer Biology. https://doi.org/10.1016/j.semcancer.2016.08.009
- PubMed Central (PMC) — National Institutes of Health. The Biology of Cancer Metastasis, Tumor Heterogeneity, and Tumor Microenvironment. https://pmc.ncbi.nlm.nih.gov/
บทความนี้อ้างอิงข้อมูลเชิงวิชาการตามหลักฐานเชิงประจักษ์ (Evidence-Based) แผนการรักษาและผลลัพธ์ขึ้นอยู่กับลักษณะทางพยาธิวิทยาและสภาวะร่างกายของผู้ป่วยแต่ละบุคคล โปรดปรึกษาแพทย์เฉพาะทางเพื่อการวินิจฉัยที่แม่นยำ